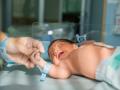
Un bebé estadounidense con una afección poco común se ha convertido en el primer paciente de la historia en ser tratado con una técnica de edición genética personalizada que brinda esperanza a otras personas con enfermedades desconocidas.
Un bebé con una enfermedad congénita incurable recibe con éxito una terapia genética experimental
La dolencia, que aparece desde los primeros días de vida, se origina por la carencia de una enzima en el hígado, impidiendo la correcta eliminación del amoniaco generado durante la descomposición de las proteínas
Un bebé con una enfermedad metabólica congénita ha sido el primero en recibir una terapia experimental y personalizada basada en la edición genética mediante la tecnología CRISPR, a la que ha reaccionado de manera positiva. No obstante, será necesario continuar el seguimiento clínico para valorar de forma completa los beneficios a largo plazo del tratamiento.
El pequeño, identificado como KJ en el estudio publicado por The New England Journal of Medicine, padece una grave deficiencia de carbamoil fosfato sintetasa 1 (CPS1), una enfermedad genética rara e incurable que afecta el metabolismo del ciclo de la urea. El caso ha sido tratado con éxito en el Hospital Infantil de Filadelfia, en colaboración con la Universidad de Pensilvania.
KJ recibió la primera dosis de la nueva terapia el pasado febrero, cuando tenía entre seis y siete meses de edad. Desde entonces, su evolución ha sido favorable. «Aunque KJ necesitará un seguimiento cuidadoso durante el resto de su vida, nuestros resultados iniciales son bastante prometedores», aseguró Rebecca Ahrens-Nicklas, médica del centro y una de las autoras del trabajo.
En los casos de deficiencia de CPS1, el tratamiento habitual consiste en un trasplante de hígado. Sin embargo, esta intervención solo puede realizarse cuando el paciente alcanza cierta estabilidad y edad, lo que implica un riesgo elevado de fallo hepático en el intervalo. En ese contexto, los investigadores comenzaron en 2023 a explorar terapias genéticas personalizadas para enfermedades metabólicas raras, lo que desembocó en el desarrollo de esta terapia dirigida a una variante específica de la CPS1.
La dolencia, que aparece desde los primeros días de vida, se origina por la carencia de una enzima en el hígado, impidiendo la correcta eliminación del amoniaco generado durante la descomposición de las proteínas. Esta acumulación puede alcanzar niveles tóxicos y provocar daños cerebrales y hepáticos severos.
Durante sus primeros seis meses, KJ permaneció ingresado bajo una dieta extremadamente restringida. Paralelamente, los científicos trabajaron en el diseño de un tratamiento personalizado que se basa en la entrega de la herramienta CRISPR mediante nanopartículas lipídicas dirigidas al hígado, con el objetivo de corregir el defecto enzimático.
Tras la dosis inicial, el bebé recibió dos aplicaciones más en marzo y abril, sin que se produjeran efectos adversos significativos. En el breve periodo desde entonces, ha mostrado avances importantes: tolera una mayor ingesta de proteínas y necesita menos medicación. Además, ha superado infecciones comunes, como un resfriado por rinovirus, sin registrar acumulaciones peligrosas de amoniaco.
Pese a estos avances, los especialistas recuerdan que aún queda un largo camino por recorrer. Los Institutos Nacionales de Salud de Estados Unidos (NIH), que financiaron parte del estudio, afirmaron que el equipo investigador se mantiene «cautelosamente optimista» respecto a la evolución del niño.
La técnica CRISPR permite realizar modificaciones precisas en el ADN dentro de las células vivas. En este caso concreto, se aplicó de forma que solo afectara a células somáticas, es decir, no reproductoras, asegurando así que los cambios genéticos no se hereden.
Los responsables del tratamiento confían en que este sea el primer paso hacia una nueva generación de terapias adaptadas a las necesidades específicas de pacientes con enfermedades genéticas únicas. «Esperamos que este niño sea el primero de muchos que se beneficien de una metodología que puede adaptarse a las necesidades» de cada paciente, señaló Ahrens-Nicklas. Por su parte, Kiran Musunuru, también autor del estudio, expresó su deseo de que otros grupos de investigación puedan aplicar esta estrategia a muchas otras enfermedades raras.
En un análisis externo, el investigador Lluís Montoliu, del Centro Nacional de Biotecnología (CNB-CSIC), calificó el caso como un ejemplo paradigmático de desarrollo de una terapia ad hoc para una mutación individual. No obstante, advirtió que «difícilmente será escalable o universalizable», ya que cada paciente presenta mutaciones distintas. Además, destacó en declaraciones al Science Media Centre que el estudio no aborda una cuestión clave: la accesibilidad y el coste real de estos tratamientos para niños con enfermedades similares.